AI geeft zorgprofessionals een slimme copiloot: snellere, nauwkeurigere diagnoses, persoonlijkere behandelingen en soepelere workflows – met minder administratie en meer tijd voor de patiënt. Je ziet concrete toepassingen in radiologie en pathologie, triage en voorspellende modellen, plus hoe je integreert met EPD/PACS en prestaties borgt met heldere metrieken. Ook komen veilig en eerlijk gebruik aan bod: mens-in-de-lus, uitlegbaarheid, bias, AVG/NEN 7510 en CE/MDR, zodat je AI verantwoord en schaalbaar inzet.

Wat is artificial intelligence in de geneeskunde
Artificial intelligence (AI) in de geneeskunde is het slim inzetten van algoritmen die patronen leren uit medische data om je te helpen sneller, nauwkeuriger en consistenter beslissingen te nemen. In plaats van vaste if-then-regels leert AI van voorbeelden: machine learning en deep learning herkennen subtiele signalen in röntgenfoto’s, CT’s en MRI’s die je met het blote oog kunt missen, terwijl natural language processing (taalmodellen) betekenis haalt uit vrije tekst in het elektronisch patiëntendossier (EPD). Zo ondersteunt AI je bij diagnosestelling, risicovoorspelling, behandelkeuze en workflow, bijvoorbeeld door triage te versnellen of administratieve lasten te verminderen. Generatieve AI kan concept-teksten samenvatten of opstellen, mits je altijd klinische controle houdt.
De kracht van AI zit in het combineren van verschillende databronnen-beelden, labwaarden, sensordata en geschiedenis-tot bruikbare inzichten aan het bed of in de poli. Tegelijk draait het om veilig en verantwoord gebruik: je borgt datakwaliteit, bewaakt privacy, voorkomt bias (vooroordelen in data) en zorgt dat beslissingen uitlegbaar blijven. Elke toepassing vraagt om strikte validatie met klinische evidence en duidelijke prestaties zoals sensitiviteit en specificiteit, zodat je weet wanneer je het resultaat mag vertrouwen. AI vervangt je niet als zorgprofessional, maar fungeert als copiloot die routinetaken overneemt en je klinische blik scherpt, zodat je meer tijd hebt voor de patiënt.
[TIP] Tip: Zorg voor hoge datakwaliteit en valideer modellen op eigen populatie.
Toepassingen van medische AI vandaag
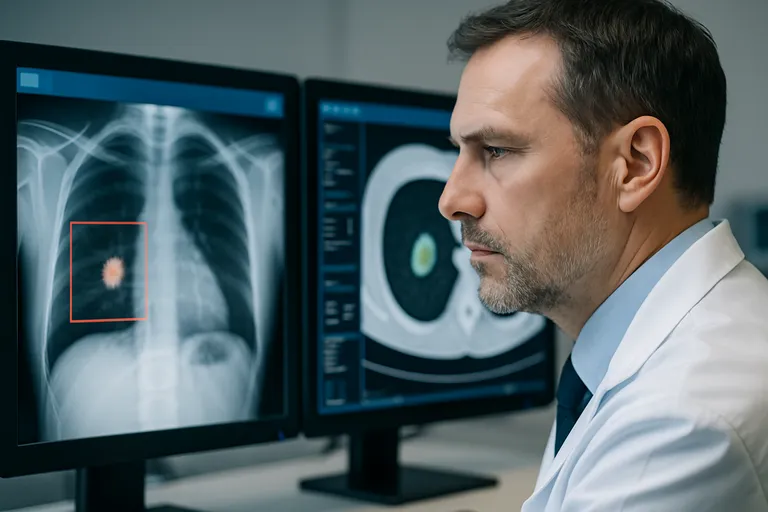
Medische AI wordt vandaag al breed toegepast om je klinische werk sneller, nauwkeuriger en beter schaalbaar te maken. In de diagnostiek helpt AI radiologie en pathologie met het opsporen van longknobbeltjes, fracturen, CVA-tekenen en verdachte cellen op digitale coupes, terwijl in de oogheelkunde diabetische retinopathie automatisch gescreend kan worden. In de kliniek draaien voorspellende modellen op EPD-data om sepsis, verslechtering op de afdeling of heropnames te signaleren, zodat je eerder kunt ingrijpen. Bij behandeling ondersteunen algoritmen het plannen van radiotherapie, het segmenteren van tumoren en het personaliseren van medicatie op basis van risico’s en comorbiditeit.
Taalmodellen vatten consulten samen, zetten spraak om in gestructureerde notities en halen relevante informatie uit vrije tekst, waardoor je minder tijd kwijt bent aan administratie. In de spoedzorg versnellen triagemodellen de juiste toewijzing van urgentie, en in de chronische zorg bewaken wearables en thuismetingen hartritme, glucose of ademhaling met automatische alerts. Ook operationeel maakt AI verschil, van bed- en OK-planning tot voorraadbeheer. In al deze toepassingen blijft je klinische oordeel leidend, met AI als copiloot die je workflow ondersteunt.
Diagnostiek en beeldvorming (radiologie, pathologie)
AI helpt je medische beelden sneller en consistenter beoordelen. In de radiologie markeren algoritmen longknobbeltjes op CT, microfracturen op röntgen en vroege CVA-signalen op CT of MRI, terwijl ze laesies segmenteren en volumes berekenen voor follow-up. Worklist-prioritering zet verdachte scans bovenaan zodat je kritieke gevallen sneller ziet, en kwaliteitscontrole spoort artefacten of slechte belichting op vóór je gaat rapporteren. In de pathologie analyseren modellen digitale coupes (whole-slide images), herkennen ze metastasen in schildwachtklieren, tellen ze mitosen en ondersteunen ze tumorgraad-classificatie, vaak met heatmaps die laten zien welke regio’s meespeelden.
Je blijft altijd aan zet: buiten de trainingspopulatie kan de prestatie dalen, dus je werkt met gevalideerde drempelwaarden, bekende sensitiviteit en specificiteit en een duidelijke integratie in PACS en LIS. Zo gebruik je AI als nauwkeurige copiloot zonder je klinische scherpte te verliezen.
Voorspellende modellen voor uitkomsten en behandelkeuze
Voorspellende modellen helpen je risico’s en te verwachten uitkomsten vroegtijdig inschatten, zodat je gerichter kunt behandelen. Ze combineren EPD-gegevens, labwaarden, vitale parameters, beeldvorming en soms wearables om kans op sepsis, verslechtering, heropname, mortaliteit of bijwerkingen te berekenen. Prognostische modellen schatten het algemene risico, terwijl behandelingsmodellen inschatten wie waarschijnlijk meer baat heeft bij optie A dan B, bijvoorbeeld met causal ML of treatment effect-schattingen.
In de workflow verschijnen adviezen als risicoscores met drempelwaarden, inclusief uitleg welke factoren het meest bijdragen en welke onzekerheidsmarge geldt. Jij houdt de regie: je let op discriminatie (AUC), calibratie en fairness, stemt drempels af op richtlijnen en capaciteit, en evalueert impact in de praktijk. Met continue monitoring op datadrift en periodieke hertraining blijft de besluitvorming betrouwbaar en relevant.
Workflow-automatisering en triage
AI neemt routinetaken uit je handen en zet de juiste patiënt op het juiste moment op de juiste plek. In de spoedzorg ondersteunt triage met realtime risicoscores op basis van vitale waarden, klachten en eerdere bezoeken, zodat je urgentie en doorverwijzing sneller bepaalt. In de dagelijkse workflow sorteert AI je worklists in EPD, PACS en LIS op klinische prioriteit, matcht verwijzingen aan de juiste specialist, plant controles automatisch in en vult conceptverslagen of coderingen voor je aan.
Intakebots verzamelen gestructureerde anamnese vóór het consult en samenvatten lange brieven tot de kern. Om alarmmoeheid te voorkomen stel je drempels en batching slim af, log je beslissingen en monitor je prestaties en datadrift. Zo verkort je doorlooptijden, verminder je fouten en houd je meer tijd over voor patiëntencontact.
[TIP] Tip: Start met één klinisch proces en definieer meetbare uitkomsten.
Implementatie in de praktijk
Succesvol implementeren van medische AI begint bij een concreet zorgprobleem en een strak ingerichte praktijk. Met onderstaande stappen ga je van idee naar een veilige, bruikbare oplossing aan het bed.
- Datakwaliteit en EPD-integratie: kies een use-case met meetbare doelen (bijv. doorlooptijd, sensitiviteit, specificiteit, foutreductie of kosten), breng workflow en beslismomenten in kaart, zorg voor consistente definities en correcte labels met zo min mogelijk missing data, koppel het model via standaarden als HL7 FHIR/DICOM aan EPD/PACS met single sign-on, rechten en audittrail, en start in “silent mode” met logging en een intuïtieve UI binnen bestaande schermen.
- Validatie en klinische evidence (inclusief metrieken): valideer gefaseerd (retrospectief intern/extern, daarna prospectief in de praktijk), rapporteer passende metrieken zoals sensitiviteit, specificiteit, AUROC/PR-AUC, calibratie (bijv. Brier), PPV/NPV en doorlooptijd/impact op fouten, en toets fairness over subgroepen en alarmmoeheid; documenteer indicaties, contra-indicaties en beperkingen.
- Adoptie en opschaling in je zorgproces: borg governance met een klinisch eigenaar, product owner en datasteward, leg SOP’s, mens-in-de-lus en escalatie vast, organiseer training en change management met feedback in de workflow, monitor prestaties en modeldrift continu (MLOps) met versiebeheer en periodieke herbeoordeling, en schaal gecontroleerd op van pilot naar brede uitrol op basis van kwaliteits- en ROI-resultaten.
Begin klein met een afgebakende pilot en een duidelijke meetlat, leer en verbeter cyclisch. Zo maak je AI aantoonbaar waardevol én veilig in je dagelijkse zorgproces.
Datakwaliteit en EPD-integratie
Sterke AI begint met schone, complete en consistente data. Je let op correcte coderingen (bijvoorbeeld SNOMED CT en LOINC), uniforme eenheden, deduplicatie en duidelijke definities van velden, zodat een model niet leert op ruis of toevallige correlaties. Labels moeten betrouwbaar zijn en herleidbaar, met versies en provenance vastgelegd. Voor integratie met je EPD koppel je via gestandaardiseerde uitwisseling zoals HL7 FHIR of DICOM voor beelden, idealiter met SMART on FHIR voor single sign-on en veilige autorisatie.
Je kiest een workflow die past: real-time events voor triage of batch voor nachtelijke scores, en je presenteert resultaten contextueel in dezelfde schermen waar je werkt. Begin met read-only en “silent” testen om foutstromen te voorkomen, monitor datadrift en logging, en leg afspraken vast over write-back, auditing en beheer. Zo houd je AI betrouwbaar én bruikbaar.
Validatie en klinische evidence (inclusief metrieken)
Onderstaande vergelijking laat zien welke validatiefase je wanneer inzet, hoe je die studie opzet en welke metrieken het bewijs leveren dat een medische AI veilig, effectief en generaliseerbaar is.
| Validatiefase / studietype | Doel | Typische studie-opzet | Belangrijkste metrieken |
|---|---|---|---|
| Interne technische validatie | Prestaties en overfitting op ontwikkeldata beoordelen | Train/val/test-splitsing per patiënt; k-fold cross-validation; bootstrapping | AUROC/AUPRC; sensitiviteit, specificiteit, F1; calibratie (Brier score, slope, intercept) |
| Externe validatie (multicenter/temporale) | Generaliseerbaarheid en robuustheid aantonen | Testen op onafhankelijk ziekenhuis/cohort; temporele split; subgroepanalyses | AUROC/AUPRC en calibratie op nieuwe data; prestatie per subgroep; kalibratieplot |
| Prospectieve klinische validatie (“silent mode”) | Veiligheid en workflow-geschiktheid toetsen zonder zorg te beïnvloeden | Model draait live maar advies niet zichtbaar; vergelijking met referentiestandaard | Concordantie/kappa; sensitiviteit/specificiteit; turn-around time; alarmbelasting |
| Klinische impactstudie (utility) | Effect op patiëntuitkomsten en beslissingen aantonen | RCT, cluster- of stepped-wedge design; vooraf gedefinieerde eindpunten | Primaire uitkomst (bv. mortaliteit, complicaties); net benefit (decision curve); NNT/NNH; ICER/kosten |
| Post-market surveillance & monitoring | Bewaken van performance, drift en veiligheid in de praktijk | Real-world data monitoring; drempels en alerts; change management bij updates | AUROC/AUPRC en calibratiedrift; false-positive rate/alert fatigue; incidentenrapportage |
Belangrijk is om van interne naar externe en uiteindelijk prospectieve en impactstudies te bewegen, met naast discriminatie ook calibratie en klinische utility als kernmetrieken. Continue monitoring borgt dat prestaties en veiligheid behouden blijven na implementatie.
Je valideert een AI-tool stap voor stap: interne validatie om overfitting op te sporen, externe validatie in andere ziekenhuizen en prospectieve testen in de praktijk, bij voorkeur met impactstudies of RCT’s. Je beoordeelt prestaties met ROC-AUC voor discriminatie, sensitiviteit, specificiteit, PPV/NPV bij klinisch relevante drempels, en calibratie (calibration slope, Brier score).
Besliswaarde toets je met decision curve analysis en net benefit, zodat je weet of het model echt helpt. Voer subgroepanalyses uit voor fairness, check generaliseerbaarheid en definieer stopregels bij datadrift. Documenteer onzekerheid en uitlegbaarheid, en monitor continu na livegang met auditlogs en periodieke herijking van drempels.
Adoptie en opschaling in je zorgproces
Adoptie begint met eigenaarschap en een helder probleem: wie voelt de pijn en wie profiteert? Je vormt een klein kernteam met klinische champions, IT en kwaliteit, traint gebruikers in de echte workflow en bouwt feedback direct in de app. Meet vanaf dag één operationele en klinische KPI’s zoals doorlooptijd, alarmbelasting en gemiste gevallen, en pas drempels aan op capaciteit en richtlijnen. Schaal gefaseerd: eerst één afdeling, dan vergelijkbare settings, met dezelfde configuratie, duidelijke fallback en support.
Regel governance voor updates, incidenten en modelwijzigingen, leg verantwoordelijkheden vast en bied korte refresh-trainingen. Maak de businesscase zichtbaar met dashboards en vier successen, zodat je draagvlak groeit en AI structureel waarde toevoegt aan je zorgproces.
[TIP] Tip: Start met een pilot, stel duidelijke criteria, betrek eindgebruikers vroeg.

Risico’s, ethiek en regelgeving
Bij medische AI draait verantwoord gebruik om drie pijlers: risico’s beheersen, ethische keuzes borgen en voldoen aan regels. Je let op bias door scheve of te kleine datasets, datadrift waardoor prestaties dalen, en automation bias waarbij je adviezen te snel volgt. Daarom werk je met uitlegbaarheid, heldere drempels en een mens-in-de-lus die eindverantwoordelijk blijft. Ethisch bouw je aan rechtvaardigheid, transparantie en proportionaliteit: leg vast waarvoor het model wél en niet bedoeld is, maak onzekerheid zichtbaar en geef de patiënt regie over gegevens. Juridisch en organisatorisch zorg je voor privacy-by-design volgens de AVG (privacywet), dataminimalisatie, een DPIA waar nodig en stevige informatiebeveiliging (bijvoorbeeld NEN 7510).
Is je toepassing een medisch hulpmiddel? Dan voldoe je aan de MDR (Medical Device Regulation), inclusief CE-markering, klinische evaluatie, risicobeheer en post-market surveillance. Richt een kwaliteitsmanagementsysteem in, log beslissingen, monitor continu op prestaties, meld incidenten en beheer updates gecontroleerd. Houd ook rekening met de EU AI Act en het risicogebaseerde toezicht dat daarbij hoort. Als je deze basis op orde hebt, groeit vertrouwen vanzelf en wordt AI een veilige, schaalbare manier om je kwaliteit van zorg merkbaar te verbeteren.
Ethisch en verantwoord gebruik: mens-in-de-lus, uitlegbaarheid en bias
Ethisch werken met medische AI begint met een duidelijke mens-in-de-lus: jij blijft eindverantwoordelijk, bevestigt of wijzigt het AI-advies en kunt het altijd overrulen. Bouw expliciete beslismomenten in voor risicovolle stappen en voorkom automation bias door het model niet automatisch te laten doorvoeren. Uitlegbaarheid betekent dat je ziet waarom een advies tot stand kwam: welke kenmerken telden mee, hoe zeker is de uitkomst en welke beeldregio’s waren bepalend (bijvoorbeeld via warmtekaarten).
Leg ook vast waar het model níet voor bedoeld is. Bias pak je aan bij de bron door representatieve data te gebruiken, prestaties per subgroep te meten en zo nodig te herkalibreren of drempels per populatie bij te stellen. Met logging, periodieke reviews en feedback van gebruikers houd je rechtvaardigheid, transparantie en veiligheid op niveau.
Privacy en veiligheid: AVG en NEN 7510
Bij medische AI bescherm je patiëntgegevens met privacy-by-design en security-by-design. Onder de AVG werk je met een rechtmatige grondslag en duidelijk doel, pas je dataminimalisatie toe, stel je waar nodig een DPIA op, leg je verwerkersovereenkomsten vast en respecteer je patiëntenrechten. Technisch versleutel je data in rust en in transit, pseudonimiseer je trainingsdata en beperk je toegang strikt tot need-to-know met sterke authenticatie.
NEN 7510 vertaalt dit naar een informatiebeveiligingssysteem: beleid, risicobeoordelingen, logging en monitoring, patchmanagement, netwerksegmentatie, back-ups en continuïteitsplannen. Je test regelmatig (bijvoorbeeld via pentests), traint gebruikers tegen phishing en hebt een helder incidentproces met datalekmelding binnen 72 uur. Met periodieke audits en lifecyclebeheer van modellen houd je privacy en veiligheid aantoonbaar op niveau.
Regelgeving en compliance: CE-markering, MDR en toezicht
AI-software die diagnose of behandeling ondersteunt geldt meestal als medisch hulpmiddel en valt onder de EU MDR (Medical Device Regulation). Voor CE-markering lever je technische documentatie aan, toon je klinische veiligheid en performance aan, en beheer je risico’s volgens ISO 14971, inclusief gebruiksvriendelijkheid en cybersecurity. De risicoklasse is vaak IIa of IIb; bij hogere klassen toetst een notified body je dossier.
Je richt een kwaliteitsmanagementsysteem in (ISO 13485), bewaakt prestaties na marktintroductie (PMS/PMCF), registreert in EUDAMED met UDI en meldt incidenten tijdig. In Nederland houdt de IGJ toezicht, in België het FAGG; zij kunnen inspecteren en handhaven. Zorg dat je wijzigingen gecontroleerd uitrolt, versies traceert en real-world resultaten continu monitort, zodat je aantoonbaar compliant blijft.
Veelgestelde vragen over artificial intelligence in medicine
Wat is het belangrijkste om te weten over artificial intelligence in medicine?
Artificial intelligence in medicine gebruikt algoritmen om klinische besluitvorming te ondersteunen, van beeldvorming en diagnose tot triage en voorspelling. Het vervangt artsen niet, vereist hoge datakwaliteit, uitlegbaarheid, CE/MDR-compliance en continue monitoring voor veiligheid en effectiviteit.
Hoe begin je het beste met artificial intelligence in medicine?
Begin met een concrete use-case met klinische eigenaar, realistische KPI’s en duidelijke baten. Check datakwaliteit en EPD-integratie, kies gevalideerde, CE-gemarkeerde tools, voer een DPIA uit, start gecontroleerde pilot, meet prestaties, borg mens-in-de-lus.
Wat zijn veelgemaakte fouten bij artificial intelligence in medicine?
Veelgemaakte fouten: slechte datarepresentativiteit, geen externe validatie, onduidelijke metrieken, negeren van workflow en EPD, ontbreken van klinisch eigenaarschap, overschatting zonder mens-in-de-lus, onvoldoende privacybeveiliging (AVG/NEN 7510), geen post-market surveillance of biasmonitoring.
